Archív článkov
Tehotenstvo a glaukómové ochorenie
Tehotenstvo a glaukómové ochorenie.
MUDr. Martina Molitorová
Glaukómová ambulancia Žilina
Žiadna štúdia doposiaľ neskúmala prevalenciu primárneho glaukómu s otvoreným uhlom v tehotenstve. Zriedkavo je PGOU diagnostikovaný v tehotenstve, častejšie otehotnie pacientka s preexistujúcim glaukómom. Priebeh PGOU sa počas tehotenstva väčšinou zlepší.
U zdravých očí dochádza k poklesu vnútroočného tlaku o 10%. Výraznejší pokles vnútroočného tlaku bol zaznamenaný u očnej hypertenzie medzi 24.- 30. týždňom. Pokles VOT počas 3. trimestra tehotenstva o 2,7 mmHg je spojený s menšou diurnálnou fluktuáciou.
Mechanizmus poklesu vnútroočného tlaku v tehotenstve je komplexný. Dochádza k zvýšeniu uveosklerálneho odtoku a poklesu episklerálneho venózneho tlaku. Acidóza počas tehotenstva znižuje produkciu komorového moku. Pri zmenenej korneosklerálnej rigidite môže dôjsť k chybám merania vnútroočného tlaku. V zornom poli zaznamenávame asymptomatické zmeny – bitemporálne zúženie ZP, koncentrické zúženie ZP, rozšírenie slepej škvrny. V tehotenstve zvýšená hladina estrogénu vyvoláva vazodilatáciu a dochádza k zvýšeniu retrobulbárneho krvného prietoku.
V priebehu pôrodu VOT stúpa priemerne o 1,4 mmHg , naopak tesne po pôrode dochádza k poklesu VOT o 3 mmHg. Tranzientná hypotenzia po väčšej strate krvi znamená zvýšené riziko progresie glaukómovej neuropatie.
Prognóza priebehu PGOU v tehotenstve je komplikovaná. Na jednej strane dochádza k zníženiu VOT, poklesu diurnálnej fluktuácie VOT, zvýšeniu retrobulbárneho krvného prietoku – čo znamená možný protektívny efekt tehotenstva na progresiu glaukómu. Na strane druhej zvýšená noncompliance, odmietanie terapie počas tehotenstva v snahe ochrániť plod môže vyústiť do progresie ochorenia.

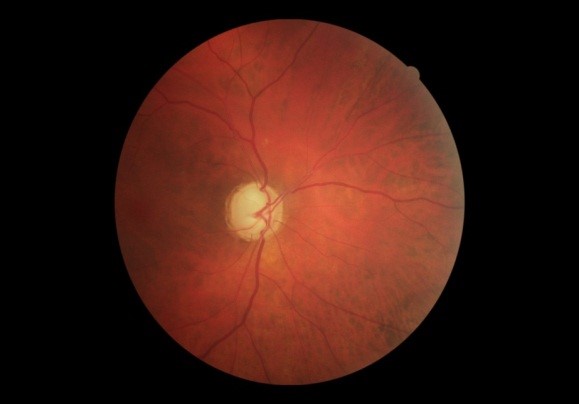
V terapii tehotných žien a pacientiek plánujúcich tehotenstvo prihliadame: na vedľajšie účinky antiglaukomatík, riziko chirurgickej intervencie a možný teratogénny efekt liečby na plod. Riziko pre matku, ktoré znamená progresiu ochorenia je v kontraste s rizikom pre plod, ktoré spôsobujú vedľajšie nežiaduce účinky liečby.
Podľa FDA klasifikácie Liekových rizikových kategórií v tehotenstve všetky antiglaukomatiká okrem brimonidínu patria do liekovej skupiny C.
Nežiaduce účinky antiglaukomatóznej terapie v tehotenstve a laktácii :
Neselektívne betablokátory : aplikovaná v 1. trimestri môžu mať teratogénny účinok, môžu vyvolať prevodné poruchy a poruchy dýchania u novorodenca, neurologické komplikácie – letargiu, zmätenosť.
Selektívny betablokátor betaxolol : bezpečnejší, menej neurologických NÚ.
Aktívna sekrécia betablokátorov do materského mliekamôže spôsobiť apnoe alebo bradykardiu novorodencov , preto je u nich nutná prísna dispenzarizácia.
Perorálne inhibítory karbonahydrázy sa nedoporučujú hlavne v 1. trimestri pre možné malformácie plodu.
Lokálne inhibítory karbonahydrázy nespôsobujú systémové biochemické zmeny. Sekrécia do materského mlieka u ľudí nebola dokázaná.
Analógy prostaglandínov : pri lokálnej očnej aplikácii nebol dokázaný vplyv na predčasný pôrod / potrat. Latanoprost, travoprost sú prekurzory liečiv – menšie celkové a lokálne NÚ ako bimatoprost. Indikované u tehotných s pokročilou formou glaukómu. Sekrécia do materského mlieka u ľudí nebola dokázaná.
Pilokarpín aplikovaný v tehotenstve môže spôsobiť zmeny perfúzie placenty, u novorodenca príznaky podobné meningitíde , ale nespôsobuje kongenitálne abnormality. Nedoporučené používanie v tehotenstve
Brimonidin nenarušuje tehotenstvo, nemá teratogénny účinok na plod. U novorodencov môže vyvolať apnoe, depresiu CNS. Sekrécia brimonidínu do materského mlieka bola dokázaná, preto je vhodné túto terapiu vysadiť u kojacich matiek
Laserová terapia :
SLT – bezpečná metóda v tehotenstve aj v období kojenia
YAG LI – bez teratogénneho efektu
Žiadne známe systémové NÚ na plod.
Chirurgická terapia : Topická kvapková anestéza je bez kontraindikácií u tehotných a dojčiacich žien. Lokálna sub-tenonská anestéza znamená menšiu systémovú absorbciu anestetika ako retrobulbárna / celková anestéza. Antimetabolity sú v tehotensteve kontraindikované pre teratogénny efekt. Používanie vnútroočných implantátov je bezpečné. V pooperačnom období je doporučovaná lokálna aplikácia erytromycínu / kategória B / . Lokálny prednisolon acetát / C / má obmedzené použitie v idikovaných prípadoch.
Plán terapie glaukómu v jednotlivých štádiách tehotenstva :
Pri plánovaní tehotenstva je dôležité poučenie pacientky : o možných NÚ liečby na plod, o rizikách prerušenia liečby, o alternatívnych možnostiach zníženia VOT pred otehotnením – laserová, chirurgická terapia.
V 1. trimestri kladieme zvýšený dôraz na minimálnu koncentrácia a dávkovanie liečiv. Brimonidín /FDA klasifikácai trieda B / najbezpečnejšia terapia v 1. tr.
V 2. trimestri je doporučovaný Brimonidín, betablokátory / monitoring pulzu a rastu plodu /, PGA sú vysadenie pri predčasných kontrakciách uteru, lokálne inhibítory karboanhydrázy / monitoring rastu plodu /.
V 3. trimestri sú optimálnou terapiou lokálne inhibítory karboanhydrázy. SLT je alternatívna terapia počas celého tehotenstva.
Názory na terapiu počas kojenia sa líšia. Americká asociácia pediatrov doporučuje v liečbe betablokátory a lokálne inhibítory karboanhydrázy, Svetová glaukómová asociácia preferuje aplikáciu lokálnych inhibítorov karboanhydrázy a analógy prostaglandínov. Brimonidín je kontraindikovaný ! pre možnú bradykardiu, hypotenziu, hypotermiu, hypotoniu, apnoe novorodencov.
Všeobecné odporúčania pre aplikáciu antiglaukomatík v tehotenstve a laktácii:
- Používať najmenšie efektívne dávkovanie a koncentráciu terapie
- Redukovať systémovú absorbciu oklúziou punkta, zavretím viečok, odsatím prebytočných kvapiek
- Kojenie ihneď po aplikácii antiglaukomatík
- Brimonidín vysadiť počas kojenia
- Laserová terapia – bezpečná alternatíva zníženia VOT
- Chirurgická terapia – bezpečnejšia v lokálnej anestéze, bez antimetabolitov
Literatúra: Razeghinejad MR, Tai YT, Fudemberg JS, Katz LJ. Pregnancy and glaucoma. Survey of Ophthalmology 2011, 56:324-335 Johnson SM, Martinez M, Freedman S. Management of Glaucoma in Pregnancy and Lactation , Survey of Ophthalmology2001, 45:449-454, Konsenzy WGA VI.
Nefarmakologická liečba glaukómu
Nefarmakologická liečba glaukómu.
MUDr.Sylvia Lea Ferková,PhD.
Klinika oftalmológie LFUK a UNBa,Bratislava
Pri glaukóme dochádza k poškodeniu oka, ale aj mozgových štruktúr dôležitých pre videnie. V patogenéze glaukómu zohráva dôležitú úlohu mitochondriálna dysfunkcia, oxidatívny stres, aktivácia glie, nestabilný očný krvný prietok a perfúzny tlak. Následné opakované ischémie a reperfúzne poškodenie vedie k bunkovej smrti. V súčasnosti nemáme k dispozícii účinné neuroprotektívum, ktorým by sme mohli svojim pacientom predovšetkým v pokročilejších štádiách glaukómu zastaviť progresiu ochorenia. Dôležité je preto hľadať aj prírodné antioxidanty a neuroprotektíva. Experimentálne štúdie dokazujú dôležitosť a možnú účinnosť rôznych substancií . Uvedené údaje sú zatial len v štádiu sledovania a budú vyžadovať ďalší výskum.
- Flavonoidy (Quarcetin, Quarcetin glycosidy) sa nachádzajú v ovocí a zelenine , vo veľkej miere v pohánke (rutin). Patria medzi antioxidanty, zametače volných radikálov a neuroprotektíva, čím ovplyvňujú oxidatívny stres, očným tlakom indukovanú smrť gangliových buniek a moduláciu zápalových procesov v astroglii.
- Vitamín B12 a jeho aktívna forma methylcobalamin. Nedostatkom vitamínu B12 môže dôjsť k megaloblastickej anémii a neuropatii (chýbanie enzýmu methionine synthasa). Predpokladá sa jeho neuroprotektívny efekt (proti indukovanej glutamátovej smrti). Pri periférnej neuropatii zlepšuje myelinizáciu axónov, regeneráciu postsynaptických neurónov.
- Kurkuma je ázijské korenie. 2000 štúdií popisuje jej antioxidačný, antibakteriálny, antivirálny, antifungálny, antiproliferatívny, proapoptotický, imunomodulačný a protizápalový efekt. Pri neurodegeneratívnych ochoreniach ako Alzheimerova choroba a glaukóm sa predpokladá antioxidačný mechanizmus redukciou defenzívnych génov a proteínov, inhibíciou nitrit oxidu, vplyvom na NMDA indukované poškodenie, glutamátové poškodenie, pôsobenie zápalových cytokínov… Pri Alzheimerovej chorobe dochádza k supresii oxidatívneho poškodenia a zápalových prejavov, ovplyvnenie tvorby Beta- amyloid peptidu. V Indii, kde sa korenie najviac používa je menej pacientov s Alzheimerovou chorobou. V oku bolo po podaní kurkumy sledované: zlepšenie zápalových prejavov v rohovke pri suchom oku (supresia zápalových cytokínov). Antikataraktový efekt sa vysvetluje zábranou volnými radikálmi indukovanej akumulácii kalcia v šošovke (75mg/kg počas 14 dní u potkanov). Zmenšenie retinálneho poškodenia pri diabetickej retinopatii zase znížením VEGF . Pri glaukóme kurkuma pôsobí proti NMDA indukovanému poškodeniu. Skúmané sú dávky 500-8000mg/deň.
- Ginkgo biloba obsahuje 60 bioaktívnych zložiek (30 nie je inde v prírode)-24% flavonoidy, 6% terpény, 7% proantokyanidiny. Ginkgo biloba je antioxidant, lapač volných radikálov,má protizápalový a neuroprotektívny účinok. Pri liečbe bolo sledované zlepšenie periférneho a cerebrálneho prietoku krvi, inhibícia trombocyty aktivujúcich faktorov. Z glaukómov len pri normotenznom glaukóme sa popisuje zlepšenie cirkulácie, pri iných typoch nebol sledovaný výraznejší vplyv na cirkuláciu. Podľa štúdií v oku dochádza k ochrane fotoreceptorov pred svetlom, redukcii ischémie, edému a nekrózy, zmenšenie progresie diabetickej retinopatie, zlepšenie indexov zorného poľa a zvýšeniu prietoku v oftalmickej artérii. Uvádza sa použitie pri kardiovaskulárnych ochoreniach, periférnych vaskulárnych ochoreniach,demencii, tinite, sexuálnej dysfunkcii a neurodegeneratívnych ochoreniach.
- Resveratrol sa nachádza v šupkách červeného hrozna. Polyfenolický antioxidant pôsobiaci ako zložka vína ale nie sirupu alebo šťavy. Konzumácia červeného vína znižuje výskyt koronárnych srdcových ochorení a degeneratívnych ochorení (hlavne v južných štátoch Európy) . Uvádza sa kardioprotekcia, neuroprotekcia, regululácia imunity, chemoprevencia rakoviny, regulácia výživy a génov dlhovekosti, antioxidatívny efekt . Ja taktiež lapač volných radikálov, má protizápalový a estrogénu podobný účinok. V oku sa predpokladá antikataraktogénny účinok, rozširovanie retinálnych arteriol a neuroprotektívny účinok (neuritídy, SM)
- Rybí tuk- 3 -omega mastné kyseliny– (Docosahexaenoická kyselina a eicosapentaenoická kyselina) nachádzajú sa v rybách ako losos, haring, makrela, tuniak, biela ryba, halibut. Cicavce nevedia 3 -omega MK syntetizovať. Zvýšený prísun v strave znižuje vnútroočný tlak a to zvýšeným odtokom tekutiny. Pri glaukóme bola zistená nižšia hladina mastných kyselín. Kombinácia mastných kyselín +B vitamín+E vitamín zlepšuje indexy zorného poľa, ochraňuje pred oxidatívnym stresom a zvyšuje očný krvný prietok. Pozor na nežiadúce účinky ako dyspepsia, predĺženie krvácania, ↑ AST,ALT a glykémie.
- Olej sojových bôbov je fermentovaná korenina z Ázie. Dôležitú úlohu majú izoflavóny v oleji sójových bôbov ( nie sojová omáčka- veľa soli a málo izoflavónov). Olej sojových bôbov pôsobí ako antioxidant, má protizápalový účinok, spomaluje progresiu vekom podmienených zmien. Doporučuje sa u kardiovaskulárnych ochoreniach, ateroskleróze, znižuje cholesterol, triglyceridy a zvyšuje HDL cholesterol.
- Zelený čaj z Číny a Indie ( nefermentovaný) obsahuje katechíny 9,4-16,2%, tanín 0,5-2,4%,kofeín 2,1-4%, vitamín C 0,1-0,4%. Zvýšený prísun tanínu (500 µM) znižuje glutamátom indukovanú smrť, má neuroprotektívny účinok. Katechíny sú hlavná bioaktívna zložka zeleného čaju, pričom účinnou látkou je polyfenolický flavonoid. Majú neuroprotektívny účinok, sú lapač volných radikálov, antioxidant, modulátor génov. Majú vplyv na rakovinu, kardiovaskulárne ochorenia, ochorenia CNS ako Parkinsonova choroba, Alzheimerova choroba a ochraňujú pred vznikom NCMP. V oku sa predpokladá menšie poškodenie fotoreceptorov svetlom, spomalenie apoptózy a zmenšenie ischémie sietnice.
- Kávové zrná obsahujú 8% fenolickú zložku. Káva pôsobí ako antioxidant, lapač volných radikálov, inhibuje lipidovú peroxidáciu a znížuje mutagenicitu.
- Čokoláda obsahuje flavanoidy. Tmavá horká čokoláda s obsahom 15-60% čokoládového roztoku má 2x viac kakaa a polyfenolov ako mliečna čokoláda obsahujúca 10-12% čokoládového roztoku. Antioxidačný efekt kakaa je vyšší ako má víno alebo zelený čaj. Pozitívne pôsobí u kardiovaskulárnych ochorení, zlepšuje vazorelaxáciu, znižuje krvný tlak, zlepšuje inzulínovú senzitivitu a zmenšuje adhezivitu a zhlukovanie trombocytov.
- Taurín je aminokyselina z tiel živočíchov. Endogénne sa tvorí v pečeni, nachádza sa v srdci, pečeni, sietnici, krvi. Pôsobenie taurínu je spojené s fyziologickými aktivitami ako je kalciový transport, má antioxidačný vplyv, ovplyvňuje neurotransmisiu, má protizápalový a cytotoxický účinok. Vekom hladina taurínu v tele klesá. Exogénny taurín by sme mohli použiť ako prevenciu vekom podmienenej degenerácie makuly, dôležitý je pre vývoj neurálneho tkaniva sietnice. Timolol podaný spolu s taurínom v kapkách znižuje vnútroočný tlak lepšie ako timolol samotný (Prof.Oláh)
- Koenzým Q-10 je mitochondriálny antioxidant dôležitý pri prenose elektrónov. Zlepšuje mitochondriálnu funkciu pri Alzheimerovej, Parkinsonovej a Huntingtonovej chorobe. Zatiaľ sa len predpokladá účinok aj pri glaukóme.
- Kyselina listová je esenciálny vitamín dôležitý pre remetyláciu homocysteínu. Nachádza sa v zelených rastlinách , chlebe a cereáliách. Pri znížení hladiny kyseliny listovej dochádza k zvýšeniu homocysteínu a tým k zhoršeniu aterosklerózy, tromboembolických ochorení, neurodegeneratívnych ochorení, homocysteín je toxický pre gangliové bunky. Exogénne podaná kyselina listová+ vitamíny B6 a B12 znižujú hladinu homocysteínu v tele o30%. Pri PEX glaukóme sa doporučuje liečba kyselinou listovou pre nízku hladinu kyseliny listovej v tele.
- Šalvia zlepšuje krvnú cirkuláciu, má vazodilatačný efekt. Pozor na kombináciu s antikoagulaciami pre možnosť zvýšenej krvácivosti (Warfarinom). Doporučuje sa pri hypertenzii, kardiovaskulárnych ochoreniach, akútnom infarkte, NCMP. Experimentálna štúdia pri glaukóme potvrdzuje, že po intravenóznom podaní extraktu dochádza k ochrane gangliových buniek, menšej redukcii axoplazmatického toku, antioxidačnému efektu, ochraňuje zorné pole, zníženiu viskozity krvi a kapilárnej vazodilatácii.
- Ďatelina červená obsahuje primárny izoflavón. Ďatelina červená je fytoestrogénom a používa sa pri iregulárnej menštruácii, menopauze, poruchách fertility. Zložka extol je účinná pre suché oko a konjunktivitídach. Zložka puerarin je betablokátor, ktorý znižuje vnútroočný tlak, zvyšuje chorioidálny prietok, znižuje hladinu VEGF a znížuje viskozitu krvi, hlavne pri diabetickej retinopatii.
- Žeňšeň je používaný v čínskej medicíne ako antidepresívum, zlepšuje mentálne funkcie, má imunostimulačný efekt na CNS a ochraňuje ischemicky postihnuté neuróny. Mixtúra žeňšeň+Gingko biloba+ „St.Johns wort“ podporuje prežitie gangliových buniek vplyvom na imunitný systém. Predpokladá sa, že rastlinný extrakt žeňšeňu má neuroprotektívny účinok na poškodené gangliové bunky a dochádza k zlepšeniu imunitnej odpovede.
- Kustovnica-Goji– v čínskej medicíne používaná na výživu pečene a obličiek, vyrovnáva Yin a Yang v tele, ochraňuje a výživuje očí. Je dokázaný vplyv na gangliové bunky a okolité gliálne bunky. Má vysoký obsah karoténu a zeaxantínu, ktoré sú antioxidant pre oko. Vysoký podiel polysacharidov je účinný proti starnutiu, má protirakovinový, cytoprotektívny, neuro a imuno modulačný efekt. Priamo je antagonista toxínov. V oku má pozitívny vplyv na makulárnu degeneráciu, ochraňuje gangliové bunky pred apoptózou. Polysacharid moduluje aktivačné procesy retinálnej mikroglie. Treba skúmať manipuláciu neuroimunitnej odpovede mikroglie a astroglie pri ochrane GB pri glaukóme. Ukazuje sa veľký potenciál kustovnice pri zábrane vzniku glaukómu, ale aj modifikácii ochorenia priamo neuroprotekciou a moduláciou glie.
- Čučoriedky obsahujú prírodný anthocyanin s antioxidačným účinkom. Predpoklad, že zlepšujú nočné videnie a kontrast senzitivitu nebol potvrdený. Predpokladá sa zmiernenie diabetickej retinopatie, VPDM a katarakty.
- Medzi ďaľšie substancie s možným neuroprotektívnym účinkom pre glaukóm patria: Pycnogenol,N -acetylcysteín,Citicoline,Carnosine,Carnitine,Glutathion,Melatonin,alfa lipoická kyselina…
- Akupunktúra sa využíva v čínskej medicíne už stovky rokov. Rovnováha Yin a Yang je dosiahnutá prúdením Qi –vitálnej sily a energie pozdľž meridiánov, na ktorých sú akupunktúrne body. Blokáda Qi spôsobuje určitú chorobu. Predpokladajú sa rôzne mechanizmy pôsobenia akupunktúry: stimulácia uvolnenia neurochemikálií-serotonínu, opiodov. Ďalšia je teória „ brány“-akupunktúrny bod interferuje s nociceptívnymi signálmi bolesti na úrovni chrbtice. Taktiež hypotalamo-hypofyzárno- adrenálna cesta ovplyvňuje moduláciu autonómneho nervového systému, neuroimunitného systému a hormonálnej regulácie a následne pôsobí na rôzne systémy v tele. Sú používané rôzne techniky, stimulácia 1-20 bodov,kombinácia s inými typmi liečby. Akupuntúra znížuje vnútroočný tlak krátkodobo ( u ľudí návrat VOT do 5 dní). V štúdiách je popisovaný vplyv na zlepšenie centrálnej ostrosti zraku, indexov zorného poľa, zlepšenie chorioidálneho prietoku, zlepšenie ERG a VEP.
- Cvičenie môže ovplyvniť vnútroočný tlak, ale aj očný krvný prietok. Izometrické cviky– bez zmeny dľžky svalu-akútne znižujú VOT prechodne (hyperventilácia, hypokapnia). Naopak vzpieranie spojené so zadržovaním dychu VOT zvyšuje. Pri pigmentovom glaukóme môže dôjsť pri cvičení k výraznejšiemu vzostupu VOT. U mladého pacienta s pokročilým glaukómom sa môže objaviť počas cvičenia aj strata videnia , takzvaný „vascular steal“ fenomén. Izokinetické cviky-dynamické (chôdza, plávanie), spôsobujú krátkodobý pokles VOT s možnou amplitúdou až 12,86mmHg. Mechanizmus poklesu VOT môže byť osmotická dehydratácia oka, zníženie produkcie komorového moku alebo hypotalamický reflex. Vplyv na očný krvný prietok je neistý. Glaukomatici by mali pravidelne športovať (aerobik), pričom sa predpokladá dlhodobé zníženie hladiny vnútroočného tlaku.
- Žiadny orgán nie je chránený pred negatívnym vplyvom chronického stresu. Počas stresu stúpa hladina kortizolu, katecholamíny, vplýva na imunitný systém. Najvyššia hladina kortizolu je ráno a po 16 hodine klesá. Chronický stres spôsobuje oploštenie tejto celodennej krivky – celý deň a noc je hladina kortizolu vyššia. Kortizol zvyšuje vnútroočný tlak. Dochádza k vazospazmu, vazokonstrikcii a zmenšeniu perfúzie terča zrakového nervu, hypoxii, zhoršeniu axonálnej funkcie a apoptóze. Trabekulum má glukokortikoidné receptory. Zvýšená produkcia kortizolu spôsobuje zmenšenie intratrabekulárnych priestorov ukladaním depozitov extracelulárnej matrix a tým aj zhoršenie odtoku komorového moku a vzostup VOT. Stres má negatívny vplyv na progresiu glaukómu, hypertonickej a diabetickej angiopatie (retinopatie). Pre ľudí vystavených chronickému stresu je doporučená meditácia a akupunktúra, pričom dochádza k zníženiu endorfínov a tým aj ochrane gangliových buniek.
Množstvo publikácií informuje o neuroprotektívnom účinku nefarmakologických prípravkov. Stále máme nedostatok informácií, štúdie sú prevažne na zvieracích modeloch a predovšetkým chýbajú štúdie na väčšom počte ľudí. Uvedené prírodné prípravky, akupunktúru a cvičenie môžeme využiť ako alternatívnu alebo doplnkovú liečbu. Do budúcnosti predstavujú nádej na zlepšenie prognózy glaukomatikov.
Literatúra:
Konsenzus WGA 7: Liečba glaukómu
Weinreb, Araie, Susanna, Goldberg, Migdal, Liebmann
Ahmedova chlopna Buletin 2019
Posledná možnosť v chirurgii glaukómu?
MUDr. Sylvia Lea Ferková, PhD., MUDr. Marta Stanislavová, MUDr.Juraj Sekáč
Klinika oftalmológie LFUK a UNB Bratislava
Úvod: Chirurgia glaukómu má viac ako 150 rokov. V roku 1856 Graefe prvýkrát urobil bazálnu iridektómiu a v roku 1867 Wecker prvú vonkajšiu filtračnú operáciu prednú sklerektómiu. Prvýkrát bola deštrukcia ciliárneho telesa robená v roku 1932. Významným medzníkom bola trabekulektómia, ktorú v roku 1968 uviedol do praxe Cairns. História drenážnych implantátov začala v roku 1967 kedy Molteno vyvinul prvý drenážny implantát, nasledovali implantáty Krupina, Baerveldta a v roku 1993 aj Ahmedova chlopňa. 21. storočie prinieslo mikroinvazívnu glaukómovú chirurgiu s početnými menšími implantátmi, ktoré sa implantajú do iridokorneálneho uhla, subchorioidálneho priestoru alebo z vonkajšieho prístupu do prednej očnej komory (Ex-Press, I-stent, Trabectome, Glaukos, Gold shunt..)
V prípade nedostatočnej kompenzácie vnútroočného tlaku (VOT) lokálnou antiglaukómovou liečbou, pri neznášanlivosti kvapiek, po zlyhaní laserovej operácie , pri zhoršovaní štrukturálnych a funkčných zmien volíme chirurgický prístup. Prvou voľbou môže byť trabekulektómia, hlboká sklerektómia, viskokanastómia alebo mikroinvazívny postup s použitím implantátu. Úspešnosť trabekulektómie v prvých rokoch po operácii je 70-92% avšak znižuje sa časom na 42-90% hlavne u sekundrárnych glaukómov [2]. Úspešnosť operácie stúpa pri použití antimetabolitov 5–FU alebo MMC. V prípade , že dôjde k zlyhaniu operácie, vzostupu vnútroočného tlaku a zhoršovaniu výpadov v zornom poli máme možnosti reoperácie. Aký postup zvoliť? Máme niekoľko možností: retrabekulektómiu s MMC,´implantovať ďalší miniimplantát,cyklodio eventuálne cyklokryokoaguláciu alebo implantáciu drenážneho implantátu.
Drenážne implantáty sa najčastejšie implantujú u sekundárnych glaukómov (neovaskulárnych, traumatických, po uveitídach), kongenitálnych glaukómoch a u refraktérnych primárnych glaukómoch. Úspešnosť operácie je charakterizovaná ako pokles VOT ≤ 21 torr, alebo zníženie VOT ≥ 15 % eventuálne 20%. Podľa štúdie Tran a kol. bolo sledované úspešné zníženie VOT u 81% pacientov po 12 mesiacoch a 64% po 24 mesiacoch od operácie[3].V retrospektívnom sledovaní výsledkov viacerých štúdií Bikbov a kol. popisujú úspešnosť operácie 43%-83%[1].
Medzi skoré pooperačné komplikácie po implantácii drenážneho implantátu patrí nadmerná filtrácia, hypotónia, plytká PK, ablácia chorioidey, malpozícia hadičky v PK, suprachoroidálna hemorágia, hemoftalmus,nedostatočná filtrácia, zvýšenie VOT,upchatie kanyly v PK alebo v mieste ventilu /krv, fibrín, sklovec/,dehiscencia rany alebo endoftalmitída. Medzi neskoré pooperačné komplikácie patrí zvýšenie VOT následkom fibrózy okolo tela chlopne, upchatie hadičky,erózia kanyly,strabizmus a diplopia,dekompenzácia rohovky,katarakta,chronická uveitída, migrácia kanyly, hypotónia a endoftalmitída.
Výsledky : Na klinike oftalmológie LFUK a UNB Ružinov sme v rokoch 2008-2017 implantovali Ahmedov drenážny implantát u 10 pacientov . Retrospektívne sme hodnotili úspešnosť operácie. Deviatim pacientom so sekundárnym glaukómom (3x po uveitíde, 2x traumatický glaukóm, 1x adnátna katarakta, 2x diabetická retinopatia, 1x amócia sietnice) bol implantovaný Ahmedov drenážny
implantát s hadičkou zavedenou do prednej komory (model S2) a jednej pacientke s kongenitálnym glaukómom a adnátnou kataraktou s hadičkou zavedenou do sklovcového priestoru (model PC7) .
Tab. 1: Súbor pacientov
| Pacient, vek pohlavie | Základná diagnóza | Predchádzajúce antiglaukómové operácie | Pooeračné komplikácie/ reoperácia |
| 1.39r.muž | Chron uveitida | Cyklodiopexia, Ex- Press | Hypotónia hyféma/ visko do PK, skrátenie hadičky |
| 2. 36r, muž | Chron uveitída | Trabekulektómia Cyklodiopexia , T -Flux | – |
| 3. 56r,muž | Kontúzia | SLT, cyklokryopexia | Hypotonia,ablácia chorioidey hemoftalmus /resutúra, visko do PK |
| 4. 71 r, muž | Kontúzia | 2x cyklodiopexia | – |
| 5. 42r, žena | Adnátna katarakta | Cyklokryopexia | Malpozícia hadičky /skrátenie hadičky |
| 6. 26r, žena | Adnátna katarakta | Trabekulotómia, cyklokryopexia | Hemoftamus,subchoroid. hemoragia |
| 7. 68r, muž | Diabetická retinopatia | cyklokryopexia | – |
| 8. 65r, muž | Amócia sietnice | 2x cyklokryopexia, Ex-press | – |
| 9. 42r, muž | Chron uveitída | Cyklokryopexia, Trabekulektómia | – |
| 10. 69r, muž | Diabetická retinopatia | 3x cyklokryopexia | hypotónia |
Súbor tvoria 2 ženy a 8 mužov s priemerným vekom 54,6 roka. Všetci pacienti podstúpili v predchádzajúcom období 1-3 antiglaukómové operácie , pričom každý z pacientov mal 1-3x cyklodeštruktívnu operáciu, 2 pacienti trabekulektómiu, 1 pacient trabekulotómiu, 2 pacienti implantáciu Ex-Press ,1 pacient implantáciu T-Flux, 1 pacient SLT . V pooperačnom období sa vyskytli u 5 pacientov skoré komplikácie: 3x hypotónia, 1x malpozícia hadičky v PK. U troch pacientov bola nutná následná chirurgická intervencia: 1x viskomateriál do PK so skrátením hadičky, 1x viskomateriál do PK a resutúra rany,1x skrátenie hadičky. U pacientky s pokročilým kongenitálnym glaukómom, u ktorej išlo o probatórnu operáciu došlo k subchoroidálnej hemorágii,hemoftalmu a zhoršeniu centrálnej zrakovej ostrosti ( CZO) na úroveň sporného svetlocitu (Tab.1).
Tab. 2: Centrálna zraková ostrosť
| Pacienti | CZO pred operáciou | CZO pri poslednej kontrole po implantácii ADI/doba sledovania |
| 11111111111111 | -1,25D sph 6/24 | Svetlocit / 8 rokov |
| 2. | -2D sph 6/24 | 6/60 / 5 rokov |
| 3. | -1D sph 6/24 | 6/18 / 5 rokov |
| 4. | 6/24 | 6/12 / 7 rokov |
| 5. | +12D sph -6D cyl 6/60 | +12D sph -6D cyl 6/24 / 5 rokov |
| 6. | Počíta prsty na 50cm | Sporný svetlocit //7 rokov |
| 7. | 6/18 | 6/18 / 1 rok |
| 8. | +9D sph 6/18 | +9D sph 6/18 / 2 roky |
| 9. | +2D sph -4D cyl 6/12 | +2D sph -4Dcyl 6/6? / 3 mesiace |
| 10. | 6/18 | 6/18 / 2 mesiace |
7 pacientov malo na konci sledovania CZO bez zhoršenia, z toho u 4 pacientov sme zaznamenali zlepšenie CZO. Jeden pacient mal CZO zhoršenú z 6/24 na 6/60 po 5 rokoch sledovania a dvaja pacienti s pokročilou glaukómovou neuropatiou po 7 a 8 rokoch sledovania mali CZO na úrovni svetlocitu a sporného svetlocitu (Tab.2).
Tab 3: Vnútroočný tlak (VOT)
| VOT pred oper. | 47 | 48 | 60 | 46 | 45 | 48 | 32 | 34 | 38 | 38 | 40.2 |
| VOT po oper. | 17 | 22 | 15 | 16 | 15 | 20 | 17 | 22 | 16 | 6 | 16,6 |
Priemerný VOT pred zákrokom bol 40,2 mm Hg, a na konci sledovania po implantácii Ahmedovho implantátu bol 16.6 mm Hg ( Tab.3) . Priemerný rozdiel VOT pred implantáciou Ahmedovho implantátu a na konci sledovania bolo 23.6 torr – zníženie VOT priemerne o 58,7% .
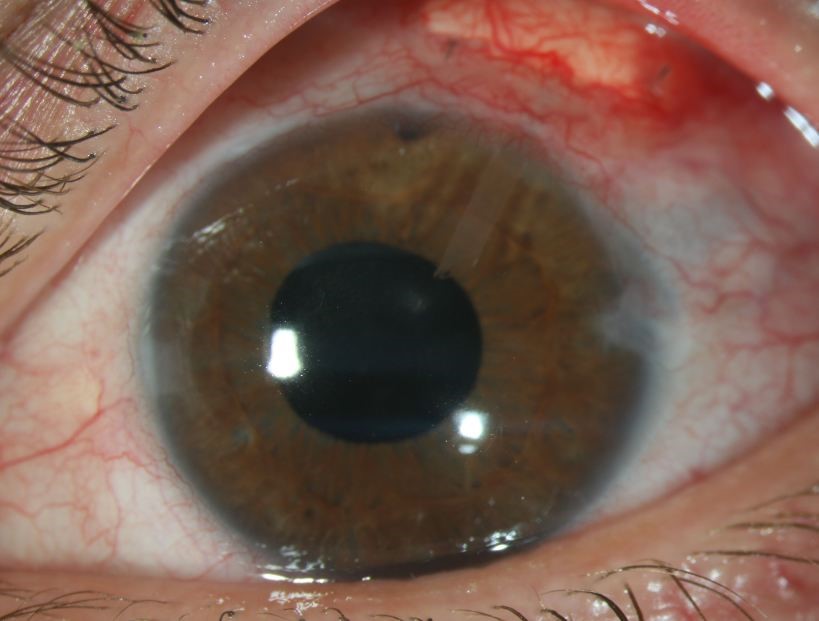
Obr.1: Nález na prednom segmente oka po implantáciii Ahmedovho drenážneho implantátu
Záver: Drenážne implantáty sú voľbou u pokročilých refraktérnych glaukómoch, u ktorých predpokladáme, že pokles VOT stabilizuje alebo spomalí zhoršovanie zrakových funkcií. Ahmedov drenážny implantát patrí spolu s Baerveldtovým implantátom k najčastejšie používaným drenážnym implantátom. Chlopňový systém, ktorý je v tele Ahmedovho implantátu znižuje riziko pooperačnej hypotónie. Štúdie poukazujú aj na možnosť použitia drenážnych implantátov ako úspešnej primárnej liečby hlavne v prípade ak je výrazné riziko zlyhania iných antiglaukómových zákrokov.
Literatúra:
1.Bikbov MM, Khusnitdinov II. The Results of the Use of Ahmed Valve in Refractory Glaucoma Surgery. J Curr Glaucoma Pract 2015;9(3):86-91.
2 Riva I et all: Ahmed glaucoma valve implant: surgical technique and complications Clinical Ophthalmology 2017:11 357–367
3. Tran DH et all: Comparison of long-term surgical success of Ahmed Valve implant versus trabeculectomy in open-angleglaucoma. Br J Ophthalmol 2009 Nov;93(11):1504-1509
Sme schopní zlepšiť očný krvný prietok?
MUDr. Sylvia Ferková, PhD.
Klinika oftalmológie LFUK a UNBa Bratislava
Oko potrebuje konštantnú perfúziu počas dynamických zmien krvného tlaku, vnútroočného tlaku a očného perfúzneho tlaku.[3]. Cievna dysfunkcia je spojená s rôznymi očnými ochoreniami, medzi ktoré patrí aj glaukóm. Stále viac štúdií poukazuje na vplyv zmien očného krvného prietoku pri patogenéze a progresii glaukómových zmien. Doteraz nie je s istotou zodpovedaná otázka, či znížený očný krvný prietok vedie ku glaukómovej neuropatii [2]. Prospektívne klinické štúdie používajúce široké spektrum zobrazovacích technológií poukazujú na redukciu choroidálneho a retrobulbárneho krvného prietoku a dysfunkciu cievnej autoregulácie u ľudí s normotenzným glaukómom a primárnym glaukómom s otvoreným uhlom [3]. Existuje hypotéza, že instabilita očného krvného prietoku vedie k opakovaným jemným reperfúznym poškodeniam ( po krátkej ischémii nastáva reperfúzia spojená so zápalovými zmenami a oxidatívnym poškodením). Pri glaukóme sú tieto poškodenia malé, ale opakujú sa. K instabilite očného krvného prietoku môže dochádzať pri fluktuácii vnútroočného tlaku, poklese krvného tlaku alebo poškodenej autoregulácii. Príčinou poškodenej autoregulácie je vaskulárny dysregulačný syndróm, a to jeho primárna forma- primárna vaskulárna dysregulácia (PVD) = vazospastický syndróm= vaskulárna endoteliopatia, vyskytujúca sa hlavne u pacientov s nižším vnútroočným tlakom. PVD má vrodený podklad a prejavuje sa od puberty so zvyšujúcou sa intenzitou. Prejavy PVD sú: studené končatiny, redukovaný pocit smädu, nízky TK, migrény, zvýšená senzitivita na lieky ( blokátory kalciových kanálov, betablokátory), dlhší čas zaspávania, dobrý čuch. Väčšinou sú to starostlivé, úspešné osoby. Reagujú vazokonstrikciou na chlad, mechanický a psychologický stres. PVD majú prevažne zdraví ľudia so sklonom k určitým ochoreniam: predná ischemická neuropatia, venózne oklúzie, centrálna serózna chorioretinopatia, Susakov syndróm, tichá myokardiálna ischémia a glaukóm. Môžeme konštatovať, že“ glaukóm sú choré oči v chorom organizme „.Dôležitú úlohu zohráva hormóm estrogén, preto prevažne PVD trpia ženy [2].
Dôležitým rizikovým faktorom pri vzniku glaukómu ( predovšetkým primárneho glaukómu s otvoreným uhlom) je nízky očný perfúzny tlak (OPT). OPT je kalkulovaný ako 2/3 stredného tlaku krvi mínus vnútroočný tlak ( OPT= 2/3 TK- VOT). Barbadoská štúdia poukazuje na to, že 41% riziko vzniku glaukómu je spojené so zníženým diastolickým perfúznym tlakom. EMGT štúdia dokazuje dôležitosť cievneho faktora v progresii glaukómu- nízky systolický perfúzny tlak, nízky systolický tlak krvi a kardiovaskulárne ochorenia boli predpokladom pre progresiu u všetkých subjektov.
Počas 24 hodinového sledovania pacientov s glaukómom bol sledovaný pokles tlaku krvi počas noci. Systémový tlak krvi bol najnižší okolo 3 hodiny nad ránom, ale len u časti pacientov došlo k abnormálnej autoregulačnej odpovedi so zhoršením schopnosti udržať si normálnu cirkuláciu. Štúdia z Thessalonik zistila, že u pacientov s poklesom diastolického krvného tlaku ( u liečených hypertonikov) pod 90 mmHg dochádza aj k zväčšovaniu C/D pomeru. Vzhľadom na zložitosť, v budúcnosti bude potrebné sledovať fluktuáciu perfúzneho tlaku meraním prietoku krvi v oblasti zrakového nervu v spojení s metabolizmom a kyslíkovou saturáciou [4].
K vaskulárnym rizikovým faktorom patria:
Vyšší vek – endoteliálna dysfunkcia-neschopnosť ciev sa rozšíriť sa, zvýšený tonus cievnej steny, vazokonstrikcia a ateroskleróza.
Chronická hypertenzia -zmeny na cievach, zvýšený odpor v cievach (naopak -občasný vzostup TK zvyšuje prietok v cievach-ochrana GB!)
Nočná hypotenzia – pri liečbe hypertenzie
Migrény– NTG- vazospasticita-porucha endoteliálnych vazoaktívnych faktorov (Endothelin- 1), vyšší vek, ženy
Hemorágie na TZN-( prelaminárna vrstva TZN a povrchová vrstva VNVS)- NTG – vazospazmus okolitých ciev, pôs. Endothelinu-1, NO, mikroinfarkty vo VNVS, defekty ZP
Diabetes– zvýšený VOT spôsobený ukladaním glukózy do trámčiny.Naopak existujú teórie, že vaskulárne zmeny pri diabete majú protektívny účinok pre glaukóm. Pri presakovaní ciev je predpoklad, že zložky séra pôsobia neuroprotektívne, VEGF pôsobí neuroptotektívne, opakované ischemické ataky trénujú sietnicu pred ďalším stresom, ktorým je glaukóm??
Imunologické abnormality– pozitívne reakcie antinukleárnych protilátok-antifosfolipidové protilátky, antifosfatidylserinové protilátky, antikardiolipínové protilátky
Sleep apnoe-hypoxia, vazospazmus, zmena nočného TK
Zvýšená viskozita krvi
Tabuľka 1 : Technológie zobrazujúce očný krvný prietok [3].
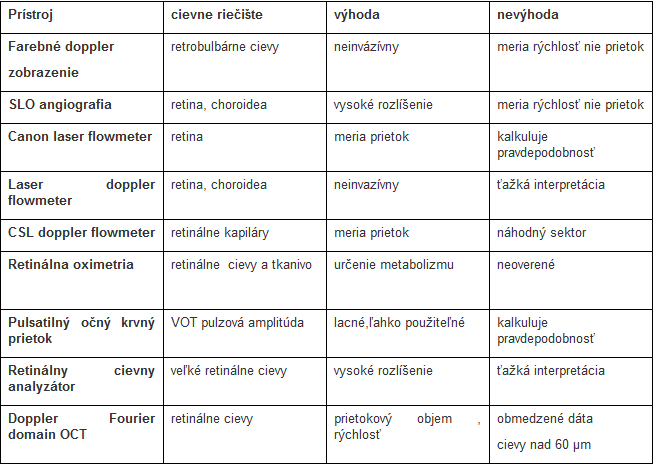
Očný krvný prietok nie je možné priamo vizualizovať, ale je možné zmerať pacientovi vnútroočný tlak a krvný tlak, z ktorých sme schopný vypočítať očný perfúzny tlak a kvantifikovať vaskulárne zmeny [1,7].Veľká väčšina štúdií popisuje pri získavaní údajov o očnej perfúzii a patofyziológii ochorenia použitie komplikovaných techník zobrazenia očnej perfúzie. V súčasnosti nemáme k dispozícii zobrazovaciu technológiu, ktorá by bola schopná merať všetky súčasti očného krvného prietoku a jeho reguláciu priamo a kvantitatívne. Prístroje nie sú určené k bežnej klinickej praxi. Najčastejšie používané prístroje, sledovaná časť cievneho riečišťa v oku, výhody a nevýhody zobrazovacej technológie sú uvedené v tabuľke číslo 1 ( tabuľka 1) [3].
Ďaľšou otázkou zostáva, či sme schopní ovplyvniť očný krvný prietok medikamentózne. Lokálne podávané kvapky musia penetrovať prednú plochu oka a dosiahnuť potrebnú koncentráciu v cievnych tkanivách. Aj pokiaľ je dosiahnutá vysoká koncentrácia vazoaktívnej látky v sklovci, ovplyvňuje len povrchové vrstvy retrobulbárneho prietoku zrakového nervu [8]. Podľa konsenzov WGA (Svetová glaukómová asociácia) z roku 2009, len inhibítory karboanhydrázy ( dorzolamid (Trusopt) a brinzolamid (Azopt)) zvyšujú očný krvý prietok a zlepšujú reguláciu krvného toku nezávisle od hypotenzívneho účinku. Úloha betablokátoru betaxololu, prostaglandínových analógov ( latanoprost, travoprost, bimatoprost,tafluprost), ale aj iných antiglaukomatík pri zlepšení očnej krvnej cirkulácie je stále rozporuplná a štúdie neukazujú na ich jednoznačnú účinnosť [5,9].
Niektoré systémovo podávané liečivá majú schopnosť ovplyvniť očný krvný prietok a jeho reguláciu. V štúdiách sa spomínajú predovšetkým centrálne pôsobiace blokátory kalciových kanálov ( nimodipine-Cordipin, Corinfar, lomerizine ), NO prekurzory ( L arginin, estrogen?) , S2 rec. antagonisti ( naftidrofuril-Enelbin retard) inhibítory angiotenzín-inhibujúceho enzýmu, inhibítory angiotenzínového receptora, inhibítory karboanhydrázy, inhibítory fosfodiesterázy 5. Medikamentózne ovplyvnenie systémového tlaku krvi môže mať výhodný ale aj negatívny efekt na očný krvný prietok( závisí to od periférneho alebo centrálneho efektu liečiva, veľkosti TK ale aj od stupňa ochorenia). Naopak súčasné užívanie diuretík a antihypertenzív zvyšuje riziko vzniku glaukómu. [6].
Neexistuje terapia , ktorá bola špeciálne vyvinutá na ovplyvnenie krvného očného prietoku. Podľa konsenzov WGA (Svetová glaukómová asociácia) z roku 2009, len inhibítory karboanhydrázy ( dorzolamid (Trusopt) a brinzolamid (Azopt)) zvyšujú očný krvý prietok a zlepšujú reguláciu krvného toku nezávisle od hypotenzívneho účinku.Nemáme dostupné informácie o tom, že zlepšením očného krvného prietoku môžeme dlhodobo ochrániť zrakové funkcie, preto použitie antiglaukomatík pre ich schopnosť zlepšiť očný krvný prietok zostáva stále na teoretickej úrovni. Sú potrebné prospektívne štúdie, ktoré nám dokážu, že zvýšením očného krvného prietoku môžeme zabrániť progresii glaukómových zmien [10].
Literatúra
Costa VP, Arcieri ES, Harris A.: Blood Pressure and glaucoma. Br J Ophthalmol.4, 2009
Flammer J., Mozaffarieh M.: What is the present pathogenetic concept of glaucomatous optic neuropathy? Survey of ophthalmology, vol 52,6, Nov, 2007
Harris A., Kagemann L, Ehrlich R., Rospigliosi C., Moore D., Siesky B.: Measuring and interpreting ocular blood flow and metabolism in glaucoma. Can J Ophthalmol vol 43,3,2008
Harris A.: Ocular blood flow in glaucoma. Review of ophthalmology,2, 2009
Harris A, Garzozi HJ, McCranor L, Rechtman E, Yung CW, Siesky B.: The effect of latanoprost on ocular blood flow. Int Ophthalmol.;29(1),2, 2008
Lesk MR et al.:The effects of systemic medications on ocular blood flow.Can J Ophthalmol, vol43,No3,2008
Martinez A., Sanchez M. : Effect of dorsolamide 2% added to timolol maleate 0,5% on intraocular pressure, retrobulbar blood flow, and the progression of visual field damage in patients with primary open-angle glaucoma: A single –center, 4-Year, open label study.Clinical therapeutics/vol 30,No 6,2008
Siesky B et al : A comparative study od the effects of brinzolamide and dorsolamide on retinal oxygen saturation and ocular microcirculation in patients with primary open-angle glaucoma. Br J Ophthalmol ,92,2008
Steigerwalt RD et al :Ocular and retrobulbar blood flow in ocular hypertensives treated with topical timolol,betaxolol and carteolo. Journal of ocular phramacology and therapeutics,vol 17, No6,2001
Stewart WC et al.:Ocular blood flow in glaucoma:the need for future clinical evidence and patient outcomes research. Br J Ophthalmol ,91, 2007
Diagnostika a progresia glaukómu v HRT II obraze
Ferková,S.
Klinika oftalmológie LFUK,Bratislava
Prednosta: Prof.MUDr.Peter Strmeň, CSc.
Úvod
Glaukómová choroba je v súčastnosti charakterizovaná ako chronická progresívna neuropatia so zmenami terča zrakového nervu (TZN), vrstvy nervových vlákien sietnice (VNV) a zorného poľa (ZP). Ochorenie vedie k strate gangliových buniek, čo spôsobuje progresívnu stratu videnia a často vedie k slepote. Podľa údajov z roku 2000 na svete trpí glaukómom 67 miliónov ľudí (z toho v Európe 9,25 milióna ľudí), pričom liečených je 4,6 – 6,9 milióna ľudí. Rozšírenosť ochorenia v rôznych krajinách varíruje od 1 – 3% populácie. V rozvojových krajinách predstavuje glaukóm 13 % zo všetkých oslepnutí [8].
Klinické aj histologické štúdie ukázali, že zistiteľné štrukturálne zmeny na TZN a VNV predchádzajú funkčné abnormality v zmysle typických zmien ZP. Poškodenie axónov gangliových buniek je ireverzibilné a výpad 12 – 53% axónov nemusí mať perimetrickú odozvu. Vzhľadom na túto skutočnosť je zavádzanie nových postupov vedúcich k skorému odhaleniu týchto zmien významné z hľadiska včasnej diagnostiky ochorenia a správnej liečby umožňujúcej dlhodobú stabilitu výsledkov [6,10]
Takmer 150 rokov od čias Helmholtza, ktorý prvý pozoroval zrakový nerv živého človeka je vzhľad TZN dôležitým faktorom pri určovaní pokročilosti glaukómových zmien. Exkavácia TZN a stenčenie neuroretinálneho lemu je indikátorom ochorenia. Pri vyšetrení vyšetrujúci musí určiť či ide o normálny alebo patologický nález na TZN, či anomálny vzhľad TZN je výsledkom glaukómového alebo iného ochorenia, ako sa líši vzhľad TZN od predchádzajúceho vyšetrenia. Vzhľadom na rozsiahlu variáciu vzhľadu TZN u rôznych zdravých jedincov, variáciu charakteru glaukómovej exkavácie a rozdielne hodnotenie TZN rôznymi vyšetrujúcimi (ale aj samotného vyšetrujúceho od kontroly ku kontrole) je klinické hodnotenie TZN oftalmoskopom obtiažne [4].
Nové zobrazovacie techniky TZN a VNV pomocou laserových digitálnych metód sú používané od 80. rokov 20. storočia a boli zostrojené na objektívne, efektívne a reprodukovateľné meranie parametrov TZN a peripapilárnej VNV. Cieľom týchto zobrazovacích metód je podanie informácie, ktorá klinikom pomôže diferencovať medzi normálnym a glaukómovým okom a detekovať progresiu glaukómového poškodenia s vysokým stupňom pravdepodobnosti. V praxi k najčastejšie používaným laserovým digitálnym prístrojom patrí : HRT II – Heidelberg retina tomograph, SLP – Scanning laser polarimeter, OCT optical coherent tomograph [4].
Na šiestom kongrese Európskej glaukómovej spoločnosti v roku 2000 glaukómoví odborníci preferovali na morfologickú diagnostiku v 48% fotografiu TZN, v 25% HRT II, v 9% SLP, v 5% OCT a v 4% fotografiu v bezčervenom svetle a v 8% ostatné techniky [7].
HRT II
HRT II je skenovací laserový oftalmoskop, pomocou ktorého získavame trojdimenzionálny obraz zadného segmentu oka. Zdrojom svetla je diodový laser 670 nm (nízkej intenzity), pričom trojdimenzionálny obraz je sériou 32 optických rezov centrovaných na TZN a perpendikulárne na optickú os od zadnej plochy sklovca po retrolaminárnu oblasť, pričom každá plocha pozostáva z 256 x 256 pixelov. Hĺbka merania je 0,5 – 4 mm. HRT II spracuje výšku povrchu v každej meranej lokalizácii, čo rezultuje v topografický obraz pozostávajúci zo 147 000 lokálnych meraní výšky. Tri základné topografické obrazy počítač spracuje a vytvorí jeden priemerný obraz štandardnej deviácie. Následne môže vyšetrujúci manuálne označiť okraje terča na vnútornej ploche sklerálneho prstenca. Po označení kontúry na okraji terča počítač spracuje stereometrické merania uprostred kontúry. Výsledkom je set stereometrických parametrov. Jednotlivé hodnoty sú merané od referenčnej plochy, čo je plocha 50 μm pod povrchom sietnice v oblasti makulopapilárneho zväzku. Oblasť pod referenčnou plochou je jamka-exkavácia a oblasť nad referenčnou plochou je neuroretinálny lem [9].
Prvé vyšetrenie
Pri prvom vyšetrení sa porovnávajú získané údaje s normatívnou databázou. Určitým subjektívnym faktorom je manuálne ohraničenie okrajou TZN, obmedzená veľkosť porovnávacieho súboru a relatívne, štatistické nastavenie hraníc norma/patológia. Napriek všetkému prvé vyšetrenie vyjadruje mieru pravdepodobnosti ochorenia.
Topografický obraz TZN je vyznačený farebne, pričom červenou je označená exkavácia a zelenou neuroretinálny lem. Reflektívny obraz je rozdelený do 6 sektorov, ktoré sú hodnotené samostatne (obr 1-Topografický a reflektívny obraz TZN pri HRT). Zelený znak označuje normálny nález v danom sektore, žltý výkričník hraničný nález a červená značka patologický nález v danom sektore- výrazné zúženie neuroretinálneho lemu. Každý zo sektorov je samostatne spracovaný a vyhodnotený v podobe stereometrických parametrov.
Najčastejšie sledované stereometrické parametre sú:
- 1.plocha terča – totálna plocha uprostred kontúry
- 2.plocha exkavácie – plocha pod referenčnou líniou
- 3.plocha neuroretinálneho lemu – totálna plocha mínus plocha pod referenčnou líniou
- 4.pomer C/D – pomer exkavácie k TZN
- 5.hrúbka VNV – rozdiel medzi referenčnou plochou a povrchom nervových vlákien na okraji TZN- stredná výška kontúry
- 6.plocha prierezu VNV– stredná hrúbka VNV znásobená dĺžkou kontúry na okraji TZN
- 7.objem exkavácie
- 8.meranie tvaru exkavácie
- 9.objem neuroretinálneho lemu
- 10.meranie variácie výšky povrchu okolo kontúry TZ
Najdôležitejšími parametrami na odlíšenie normálneho nálezu na TZN a glaukómového TZN sú merania tvaru exkavácie, objemu neuroretinálneho lemu a meranie variácie výšky povrchu okolo kontúry TZN [1,2]. Veľká variabilita v tvare a veľkosti TZN v normálnej populácii a úzky vzťah medzi veľkosťami terča, neuroretinálneho lemu a exkavácie môže negatívne ovplyvniť schopnosť rozlíšiť fyziologický od glaukómového terča. Exkavácia je trojdimenzionálny útvar. U pacientov bez glaukómu je TZN buď bez exkavácie alebo je exkavácia plytšia, pomerne okrúhleho tvaru a centrálne uložená. U pacientov s glaukómom je exkavácia hlbšia, má ostro klesajúce steny, často zvonovitého tvaru [1]. Pri glaukóme strata retinálnych gangliových axónov zapríčiňuje zmenu v tvare TZN zmenšením neuroretinálneho lemu hlavne na hornom a dolnom póle TZN čím dochádza k vertikálnemu zväčšeniu exkavácie alebo hornému a dolnému zárezu. Väčšina glaukómových exkavácií má nepravidelný tvar a sú excentrické [3]. Viacerými štúdiami bolo zistené, že na rozsah glaukómových zmien nemá vplyv veľkosť TZN. Pri veľkých TZN môže byť normálnym nálezom aj väčšia exkavácia. Malý TZN obsahuje nahustenejšie nervové vlákna, preto aj menšia exkavácia je suspektná z glaukómového ochorenia.
Pri vyšetreniach pomocou HRT II sa môžeme stretnúť s atypickými nálezmi ako je edém TZN, drúzová papila, jamka TZN a rôzne kongenitálne anomálie TZN. V takýchto prípadoch je možné prístrojom HRT II obrazy len dokumentovať, prípadne sledovať nálezy v čase. Neslúži nám v týchto prípadoch na hodnotenie glaukómových zmien.
Pri HRT II ide o nepriame meranie vrstvy nervových vlákien. Rozsah exkavácie TZN môže byť zmenšený vradením ciev na TZN k neuroretinálnemu lemu [7]. Pri koncentrickom type exkavácie je dôležitý výsledok HRT II vzhľadom na to, že v perimetri je dlho normálny nález. Pri vysokej myopii citlivosť veľmi kolíše, môže byť falošne pozitívny výsledok. Pri senilnom type glaukómu je exkavácia plochá, a aj pri pokročilom glaukóme je často negatívny nález na HRT II. Na meranie majú vplyv vysoké refrakčné chyby, katarakta, úzka zrenica, kedy môže byť neostré zobrazenie TZN a tým aj získané falošné, často nehodnotiteľné výsledky.
V programe HRT II si možno vybrať multivariačnú analýzu , diskriminantnú analýzu a najčastejšie využívanú Moorfieldskú regresnú analýzu.
Moorfieldská regresná analýza podáva aktuálny obraz o stave TZN v jednotlivých 6 sektoroch v porovnaní k normatívnej databáze. Porovnáva sa percentuálny pomer oblasti neuroretinálneho lemu (zelený graf) ku oblasti exkavácie TZN (červený graf).
HRT II je dôležitý na preperimetrickú detekciu glaukómových zmien. Predchádza zmeny v perimetri o 3 roky. Hodnota len jedného vyšetrenia v diagnostike glaukómu je nízka. HRT II pomáha v popise parametrov TZN a stanovení základných hodnôt, ale neurčuje diagnózu. Dôležitejšia je detekcia zmeny TZN v čase [5].
Opakované vyšetrenia-hodnotenie progresie
Pri opakovanom vyšetrení dochádza k porovnaniu s predchádzajúcim vyšetrením, eliminuje sa subjektívny faktor a nepracuje sa s normatívnou databázou. Vyšetrenie na HRT II je reprodukovateľné a výsledky korelujú s histologickými nálezmi [1,2].
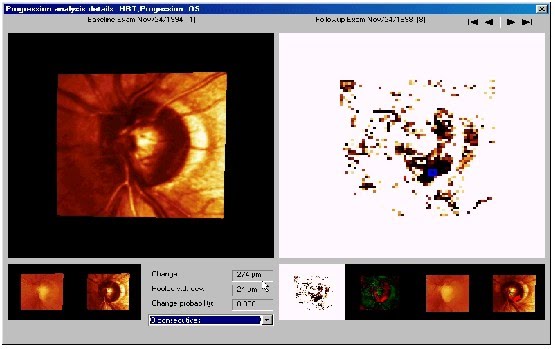
Topografická analýza progresie je možná až po 3 vyšetreniach pacienta. Pokiaľ má pacient viac ako 3 vyšetrenia počítač porovnáva tri následné vyšetrenia. Detekcia glaukómových zmien je založená na diskrepancii parametrov TZN po spracovaní topografických diferenčných obrazov – superpozícia obrázkou, na spracovaní mapy možných zmien a následnej kalkulácii významnosti zmeny. Zmenené regióny sú v topografickom obraze označené červenou ( vysoká depresia ) alebo zelenou (vysoká elevácia). Na minimalizáciu možných odlišností pri opakovanom meraní je v programe počítača zabudovaná normalizácia korekciou posunu a rotácie medzi obrazmi, korekcia zväčšenia, výšky, naklonenia obrazov. Zväčšenie je závislé od zmien refrakcie, akomodácie, katarakty. Posun obrazov a zmeny perspektívy sú dané hlavne chybnou centráciou kamery. Po normalizácii sú topografické obrazy porovnané. Kontúrová línia TZN robená pri prvom vyšetrení je prenesená automaticky do nasledujúcich vyšetrení, je na identickom mieste.
Štatisticky významná je zmena v súvislej oblasti rozsahu 20 super-pixelov ( 20x (4×4) pixel).
Kvantifikácia progresie je robená porovnávaním stereometrických parametrov, pričom už 5% variabilita výsledkov je detekovateľná. Progresiu môžeme sledovať aj v grafickom zobrazení – grafe progresívnej analýzy, pričom stereometrické parametre sú normalizované do rovnakej škály a sú uložené do diagramu pozdľž osi, pričom poukazujú na trend zmeny. Zníženie parametrov o 0,05 po troch meraniach označuje už signifikantnú odchýlku [1].
Sledovanie funkčných a morfologických zmien pri glaukóme
Na klinike oftalmológie LFUK v Bratislave v rokoch 2003-2006 prebieha štúdia zameraná na dlhodobé sledovanie funkčných a morfologických zmien pri glaukóme. Funkčné zmeny sú sledované na perimetri Octopus 101 a morfologické pomery a zmeny TZN na prístroji HRT II. Zcelkového počtu pacientov vyšetrených na HRT II bude vybraná skupina 50-70 pacientov s primárnymi formami glaukómu, u ktorých bol okrem základného očného vyšetrenia každých 6 mesiacov vyšetrený perimeter aj HRT II. Získané výsledky budú štatisticky spracované a bude hľadaná korelácia medzi jednotlivými parametrami získanými HRT II a perimetrom. Zámerom štúdie je potvrdenie úlohy prístrojov v diagnostike glaukómu, sledovaní progresie ochorenia a následne správnej indikácii konzervatívnej liečby glaukómu, ale aj včasnej indikácii chirurgického zásahu.
Záver
Hodnota len jedného vyšetrenia pomocou HRT II v diagnostike glaukómu je nízka. HRT II pomáha v popise parametrov TZN a stanovení základných hodnôt, ale neurčuje diagnózu. Dôležitejšia je detekcia zmeny TZN v čase [5]. HRT II je v súčasnosti jediná technológia sledujúca progresiu zmien v longitudinálnych štúdiách. Kalkuluje reálnu zmenu, nezávisle od kontúry a referenčnej línie.
Literatúra
1. Chauhan, B.C., Blanchard, J.W., Hamilton, D.C, Le Blanc,R.: Technique for detecting serial topographic changes in the optic disc and peripapillary retina using scanning laser tomography. Invest Ophthalmol Vis Sci, 41,2000,s.775-782.
2. Greaney, M.J., Hoffman, D.C., Garway –Heath, D.F.,Mamdoub,N.,Coleman,A.L., Caprioli,J.: Comparison of optic nerve imaging methods to distinguish normal eyes from those with glaucoma. Investigative ophthalmology& visual science, 43, 2002,s. 140-145.
3. Iester, M.,Swindale, V.N., Mikelberg, F.S.: Sector-based analysis of optic nerve head shape parameters and visual field indices in healthy and glaucomatous eyes. Journal of Glacoma,6,1997,s. 371-376.
4. Kloizman, P.T., Schuman,S.J. : Disc analysis s. 7.1-7.6 v Yanoff,M..,Duker,J.S .Ophthalmology, Mosby international Ltd,1999,1616s.
5. LeBlanc,R.P.,Soares,A.S.:Heidelberg retina tomograph and the management of glaucoma.Highlights of ophthalmology ,31,2003,s. 21-26.
6.Lešták ,J., Pašta ,J., Pešková, H.: Metody vyhodnocení zorného pole. Čs. oftalmol, 4,1997,s. 269-275.
7. Mardin,CH.Y., Jünemann,A.G.M.: The diagnostic value of optic nerve imaging in early glaucoma. Curr Opin Ophthalmol,12, 2001,s. 100-104.
8. Michelson, G.,Grohn, M..J.M.: Screening models for glaucoma. Curr Opin Ophthalmol,12, 2001,s: 105-111.
9. Miglior,S.,Casula,M.,Guareschi,M.,Marchetti,I,Iester,M.,Orzalesi,N.: Clinical ability of Heidelberg retinal tomograph examination to detect glaucomatous visual field changes. Ophthalmology, 108, 2001,s. 1621-1627.
10. Skorkovská, Š.,Stará, Š.,Kočí,J.: Hodnocení zmen zorného pole u glaukomu pri vyšetření bílými stimuly. Čs. Oftalmol., 59,2003,s. 28-32.
Diagnostika a progresia glaukómu v HRT II obraze Read More »
